Personalisierte Medikation durch digitalen 2+3D-Druck
http://doi.org/10.24945/MVF.06.20.1866-0533.2262
>> Bereits seit mehreren Jahren werden die Fortschritte durch Digitalisierungsansätze in der Medizin publiziert. Sei es die Integration von künstlicher Intelligenz, Robotik oder auch der Digitaldruck von zum Beispiel Implantaten. Insbesondere in Covid-19-Zeiten zeigt sich, dass Digitalisierungsansätze notwendige Prozesse durchaus effizienter gestalten können, wie es beispielsweise für telemedizinische Ansätze beschrieben ist. So führt dieser Trend zur Digitalisierung zunehmend auch zu weiteren Möglichkeiten der Individualisierung und der Personalisierung. Dies alles, um in der Arzneimitteltherapie Präzision, personalisierte Medizin und damit auch Patientenzentrierung weiter voranzutreiben.
Wenn der gesamte Prozess von der Diagnose zur Therapie nun betrachtet wird, so wird schnell klar, dass es im Rahmen der Pharmakotherapie seit geraumer Zeit ein großes Maß an Individualisierung bzw. Personalisierung gibt. So macht beispielsweise eine Trastuzumab-Therapie bei Frauen nur dann Sinn, wenn sie HER+ diagnostiziert sind. Im Rahmen der intravenösen Zytostatika-
Therapie wird die Dosis der verabreichten Pharmaka u.a. mit Hilfe von Vitalparametern ermittelt, auch in der Insulin-Therapie des Diabetes Mellitus Typ I wird die Menge an Insulin gespritzt bzw. mittels Pumpe zugeführt, die der individuelle Patient realiter benötigt. Im Bereich der Pharmakotherapie mit festen, oralen Arzneiformen – dies sind weltweit immerhin annähernd 2/3 des Marktes – kann dies nicht in ausreichendem Ausmaß geschehen.
Wenn wir den Blick nach vorne richten, dann zeigt sich, dass auch bei den zu erwartenden Innovationen vor allem auf Tabletten und Kapseln fokussiert wird. Der Herstellprozess von Tabletten und Kapseln ist auf einen hohen Durchsatz ausgelegt, welcher zu standardisierten Größen führt. Einzige Möglichkeit für eine andere Dosierung bzw. Stärke ist die Halbierung, Drittelung oder sogar Vierteilung durch sogenannte Bruchkerben, was jedoch nicht bei allen Pharmaka möglich ist. Eine exakte Stärke bzw. Dosis entsteht dabei nicht, Mediziner müssen mit den Stärken arbeiten, die verfügbar sind, eine Individualisierung, wie sie aus der Chemotherapie oder anderer Infusionstherapien bekannt ist, ist de facto so gut wie nicht möglich. Dies ist durchaus kritisch, da für diverse Wirkstoffe nicht nur eine enge therapeutische Breite beschrieben ist, sondern darüber hinaus zahlreiche Arzneistoffe eine starke Abhängigkeit von z.B. der Leber- oder Nierenfunktion zeigen und eigentlich genau auf die jeweilige individuelle Situation der Patienten abgestimmt werden müssten. Es zeigt sich bei einigen Wirkstoffen zudem eine hohe inter- und intraindividuelle Variabilität (z.B. Immunsuppressiva Everolimus, Tacrolimus), so dass die Dosis bzw. Stärke des Arzneimittels nicht nur jeweils neu kalkuliert werden muss (dies geschieht mit Hilfe der vorgeschriebenen Talspiegelmessung), sondern eigentlich auch exakter gegeben werden müsste, als dies durch gepresste Tabletten möglich ist.
Ein weiterer relevanter Faktor im Rahmen der Pharmakotherapie ist die bei den meisten Indikationen mangelnde Adhärenz der Patienten. Wichtige Gründe hierfür sind unter anderem komplexe Therapieschemata, unerwünschte Arzneimittelwirkungen und eine Vielzahl an einzunehmenden Arzneimitteln. So nehmen in Deutschland über 15 Millionen Menschen mehr als drei Tabletten täglich ein, Silver Ager kommen auf einen täglichen Konsum von bis zu 15 Tabletten. Menschen mit chronischen Erkrankungen repräsentieren der WHO zufolge 80% der Krankheitslast in den meisten OECD-Ländern. Wenn in Betracht gezogen wird, dass Dreiviertel aller Menschen in den westlichen OECD-Staaten über 65 Jahre unter mehr als einer chronischen Erkrankung leiden und die meisten davon zur Behandlung ihrer Erkrankung Arzneimittel einnehmen, so wird klar, dass hier durchaus Probleme auftreten können. Einige Zahlen visualisieren dies: Belastbare Schätzungen gehen davon aus, dass in Deutschland jährlich circa 500.000 Hospitalisierungen durch eine inadäquate Arzneimitteltherapie stattfinden und etwa 50.000 Menschen jährlich an den Folgen inadäquater Pharmakotherapie sterben.
Aus ökonomischer Sicht belaufen sich die Kosten für Non-Compliance auf ca. 10 Milliarden Euro in Deutschland, in den USA werden die Kosten auf ca. 300 Mrd. US-Dollar geschätzt. Der gesamte Zyklus von der Herstellung der Pharmaka hin bis zur Nutzung des Arzneimittels zeigt darüber hinaus große Ineffizienzen. Belastbare Untersuchungen gehen davon aus, dass mehr als 50% der produzierten Arzneimittel nicht dem gewünschten Zweck – nämlich der Einnahme durch den Patienten – zugeführt werden. Der Herstellungsprozess an sich, nicht vorhandene Adhärenz bzw. Compliance sowie die durch die Pharmaindustrie in hoher Stückzahl produzierten Tabletten und Kapseln (zur Erlangung eines sehr günstigen Stückkostenpreises) und zudem in großen Blistern verpackt, führt am Ende nicht zwingend zu einer effizienten Allokation der Arzneimittel.
Eine große Anzahl an Arzneimitteln wird schließlich nicht dem Patienten zugeführt, bzw. gelangt nicht in diesen, sondern wird in unterschiedlichster Weise vernichtet, die Kosten des Pharmamülls können sich durchaus auf ca. 7 Milliarden Euro per annum – alleine in Deutschland – belaufen. Ein aktuelles Problem, welches zunehmend durch die Covid-19-Situation weltweit katalysiert wird, kommt hinzu. Seit einigen Monaten besteht eine zunehmend hohe Nicht-Lieferfähigkeit von Arzneimitteln. Dies sicherlich auch bedingt durch die mittlerweile sehr konzentrierte Herstellung der Wirkstoffe in Asien. Insbesondere die Moleküle, welche für die Synthese von Arzneistoffen benötigt werden, kommen fast ausschließlich aus China und Indien. Es ist zu vermuten, dass eine sichere und flächendeckende Versorgung mit Arzneimitteln so sicherlich dauerhaft nicht gewährleistet werden kann.
Digitale Herstellungsverfahren: 2D-/3D-Druck von Arzneimitteln
Digitale, auch additive Herstellverfahren erzeugen hierbei eine vielseitige Wertschöpfung und stellen einen wichtigen Schritt hin zu einem kosteneffizienten Gesundheitswesen dar. In den letzten Jahren wurden weitere Fertigungsmethoden entwickelt, um feste Darreichungsformen (wie z.B. Tabletten und Kapseln) zu realisieren. Hierbei werden die Prozessschritte der Tablettenherstellung wie Granulieren, Sieben, Trocknen und Pressen durch alternative Prozessschritte ersetzt. Dabei eröffnen die digitalen Herstellverfahren, wie der 2D- oder 3D-Druck neue Möglichkeiten der dezentralen Herstellung von Arzneimitteln. Konkret, der Herstellung in (Krankenhaus-)apotheken, Compounding- oder auch Blisterzentren.
Der 2D-/3D-Druck hat sich bereits bis zur bevorstehenden Zulassungsreife entwickelt. Einerseits können Elemente des Gesundheitsmanagements wie Diagnose, Prävention, Verschreibung, Therapie und Therapiefortschritt in Echtzeit an die Herstellung kommuniziert werden. Ferner können via Druckherstellung Chargengrößen von einer einzelnen Tablette (batch-size-one) realisiert werden.
Der 2D- und 3D-Druck bietet viele relevante Neuerungen und ist verglichen mit der konventionellen Entwicklung und Herstellung von Festformen wie z.B. Tabletten oder Kapseln vorteilhaft. Vorteile liegen in dem geringeren Auftreten von Neben- und Wechselwirkungen, der schnelleren und bedarfsgerechten Bereitstellung der Therapeutika sowie auch der schnelleren und effizienteren Forschung und Entwicklung neuer Medikamente. Auf alle drei Themen gehen wir hier näher ein.
Geringere Neben- und
Wechselwirkungen
Der bisherige Ansatz „one-size-fits-all“ der Pharmaindustrie ist nicht mehr zwingend zeitgemäß, da (patho-)physiologische Aspekte (wie z.B. eingeschränkte Nieren- oder Leberfunktion), Arzneistoff Interaktionen, Herausforderungen im Rahmen der Adhärenz bei der Behandlung nicht konsequent berücksichtigt werden können. Auch metabolisieren Patienten den verabreichten Wirkstoff unterschiedlich schnell. Das heißt, dass manche Patienten mehr, andere weniger Wirkstoff für den optimalen Therapieerfolg brauchen. Ein Nichtadaptieren kann zu einem Versagen der Therapie oder aber einer nicht hinreichenden Wirkung bzw. zu unerwünschten und auch therapielimitierenden unerwünschten Wirkungen führen. Zusätzlich können nahezu beliebige Wirkstoffkombinationen verbunden mit jeweils individuellen Freisetzungseigenschaften in der patientenindividuellen Dosis bzw. Stärke hergestellt werden (Compounden von Tabletten, Flexdose Polypill). Durch den 2D- und 3D-Medikamentendruck kann damit für jeden Patienten die ideale Dosis gedruckt und damit die Anzahl der eingenommenen Tabletten sowie die Neben- und Wechselwirkungen reduziert werden.
Schnelle Bereitstellung der
Medikation nach Bedarf
Schätzungsweise mehr als 50% der festen Arzneistoffe werden heute ungenutzt verworfen. Dies liegt einerseits an der nicht an den Patienten-Bedürfnissen ausgerichteten Massenproduktion und Lieferung sowie an einer Medikamenten-Abgabe in festen Abgabegrößen (in Deutschland N1-N3). Andererseits kommt es unter anderem durch mangelnde Patientenorientierung immer wieder zu Medikamentenengpässen. Diese werden zudem auch durch die starke Oligopolisierung insbesondere im Herstellungsprozess von generischen Wirkstoffen und Arzneimitteln hervorgerufen. Werden Arzneimittel individuell gedruckt, dann findet das Compounding direkt in den Apotheken statt. Der Pharma-Drucker arbeitet nach Dateiinhalten, die an einem Drucker in der Apotheke gesendet werden und sich dann effizient verarbeiten lassen. So können Rezepte und Behandlungsregimes in Druckserien transformiert und individuell abgestimmt werden. Somit wird es möglich, Patienten nicht nur nach Altersgruppen (Kinder, Erwachsene, Senioren etc.) zu behandeln, sondern Therapien und Medikationen auf eine bestimmte Person und insbesondere auf den individuellen Behandlungsfortschritt abzustimmen. In Konsequenz sollten so Gesamttherapiekosten signifikant sinken.
Kostengünstigere und schnellere Forschung und Entwicklung neuer Medikamente
Die Arzneimittelentwicklung ist vermehrt zu einem zeit- und kostenintensiven Vorhaben geworden. In frühen Entwicklungsphasen müssen vorläufige Formulierungen entwickelt und anschließend in klinischen Studien getestet werden. In den klinischen Phasen, in denen die Anforderungen an die pharmazeutische Qualität durch die Anwendung am Menschen noch weitaus höher als bei Tierstudien ist, werden beispielsweise zur Dosisfindung diverse Wirkstärken, gegebenenfalls kombiniert mit einer Vergleichs- oder Kombinationsmedikation benötigt. Die zeitnahe Bereitstellung von Kleinstmengen in der Versorgung mit Studienmedikation via digitaler Drucktechnologien generiert daher einen relevanten Vorteil. Durch die Technologie des digitalen Drucks von Arzneimitteln können alle diese Varianten zu einem Minimum an Kosten entwickelt, produziert und auch jederzeit modifiziert werden, und das bei stark reduziertem Prüf- und Freigabeaufwand.
Wenn es um die orale Applikation von Wirkstoffen im Massenmarkt geht, dann sind konventionell hergestellte Tabletten auch heute noch die Arzneiform der Wahl. Sie lassen sich in sehr großen Stückzahlen sehr kostengünstig fertigen und zeigen eine ausreichende Lagerstabilität. Die Freisetzungskinetik kann durch entsprechend geeignete Formulierungen beeinflusst werden. Eine Individualtherapie lässt sich mit im industriellen Maßstab hergestellten Tabletten jedoch nicht realisieren.
Tablettenformulierungen sind komplexe Systeme aus einer Vielzahl an Hilfsstoffen, die die unterschiedlichsten Funktionen erfüllen. Aus den Tablettenformulierungen wird anschließend in mehreren Prozessschritten entweder eine Pulvermischung oder ein Granulat hergestellt und diese dann unter GMP-Bedingungen auf Rundläufertablettenpressen mit einem Ausstoß von mehreren hunderttausend Tabletten pro Stunde verpresst.
Die Produktion kleinster Tablettenchargen mit individuellen Dosierungen, individuellen Wirkstoffkombinationen oder gezielten, auf ein Individuum angepassten Freisetzungsverhalten ist in diesem Rahmen wirtschaftlich kaum möglich. Aufgrund der Kosten und Größe selbst der kleinsten Geräte ist eine solche Herstellung andererseits in Apotheken ebenfalls unrealistisch.
In der modernen Herstellung von oralen Darreichungsformen mittels der 2D- und der 3D-Drucktechnologie werden eine Reihe unterschiedlicher Druckverfahren eingesetzt. Diese haben unterschiedliche Vor- und Nachteile und stellen die Pharmaentwicklung vor unterschiedliche Herausforderungen. DiHeSys Digital Health Systems hat ein System aus Drucker, Druckkopf, Tinten bzw. Filamenten und Software entwickelt, welches bereits in Kürze sowohl in ambulanten wie auch in stationären Projekten zum Einsatz kommen wird. Bevor wir einen Blick auf die konkrete Anwendung werfen, sei zunächst grob die Verfahrenstechnologie darstellt.
Das 2D-Druck-Verfahren
von Arzneimitteln
Im Bereich des 2D-Druck-Verfahrens in Apotheken unter der Überschrift der Individualisierung bzw. der Personalisierung der oralen Pharmakotherapie ist das „Drop-on-demand“-Verfahren relevant. Bei diesem Verfahren geht es technologisch um die Verwendung von flüssigen, stabilen Formulierungen, den sogenannten Tinten, sowie einem bedruckbaren, wirkstofffreien Substrat (ODF, oral dispersible film), auf welches die wirkstoffhaltige Tinte der individuellen Verordnung des Arztes folgend aufgedruckt wird.
Herausforderungen, die sich über alle Verfahren des 2D-Druckes stellen, sind die Löslichkeit der verwendeten Wirkstoffe und ihre Stabilität in Lösung. Je nach Auswahl des Druckverfahrens muss die Wirkstofflösung bestimmte Anforderungen, wie zum Beispiel Viskosität oder Dampfdruck, erfüllen. Und auch die Oberflächenenergie der Tinte, wie auch des Substrates spielen hier eine entscheidende Rolle für die Benetzbarkeit. Die Entwicklung des Substrates muss z.B. hinsichtlich Reißfestigkeit für die Anforderungen der einzelnen Verfahren angepasst werden.
Zudem bietet die Technologie u.a. die Möglichkeit, inkompatible Wirkstoffe gemeinsam auf ein Substrat zu drucken. Ein Compounden von API (active pharmaceutical ingredient, Wirkstoff) in der Dosis bzw. der Stärke, die der Patient benötigt, ist also realisierbar.
Für die Verwendung dieser Technologie muss für jeden Wirkstoff eine spezifische Tinte entwickelt werden, gegebenenfalls auch geeignetes Substrat, um die Anforderungen an Wirkstoffbeladung, Viskosität, Ober-
flächenenergie etc. zu erfüllen. Des Weiteren sind die Parameter des Druckprozesses wie z.B. Tropfengröße, Druckgeschwindigkeit zu entwickeln und zu optimieren. Die Technologie ist bezüglich ihrer Auftragsmenge vom Wirkstoff nach obenhin limitiert, so dass diese Verfahren hauptsächlich für niedriger dosierte Wirkstoffe (in toto maximal ca. 40mg) einen signifikanten Vorteil bietet.
Das 3D-Druck-Verfahren
von Arzneimitteln
Heutzutage ist die Verwendung von 3D-Druckern in Industrie und Forschung zur Herstellung von Modellen, Prototypen und mittlerweile auch zur Serienfertigung z.B. im Bereich der Luftfahrt oder auch Medizin- und Zahntechnik bereits etabliert. Wie auch bei den 2D-Druck-Verfahren stehen verschiedene Techniken für das Drucken drei-dimensionaler Objekte zur Auswahl.
Für alle Verfahren wird im Vorfeld des Druckes ein 3D-Modell am Computer entworfen, das sogenannte Computer-Aided Design (CAD). Dann werden die Daten in einen STL file übersetzt und an den 3D-Drucker übermittelt, wo das gewünschte Objekt nun Schicht für Schicht aufgebaut wird.
Zwei Verfahren werden aktuell für die Herstellung oraler Darreichungsformen verwendet. Zum einen das Binder Jetting Verfahren und zum anderen das Fused Deposition Modeling (FDM).
Beim Binder Jetting Verfahren wird eine Pulver- oder Granulatschicht mittels einer Walze auf den Drucktisch aufgebracht. Anschließend wird mit Hilfe eines Druckkopfes ein Bindemittel auf definierte Stellen aufgetragen. Der Druckkopf lässt sich mit dem eines Tintenstrahl-Druckers vergleichen. Durch das Bindemittel verkleben die Partikel des Pulvers bzw. Granulates. Anschließend wird der Drucktisch auf eine definierte Schichtdicke abgesenkt und eine weitere Schicht des Pulvers aufgebracht, welche wiederum mit dem Bindemittel benetzt wird. Dadurch verkleben die Partikel nicht nur untereinander, sondern auch mit der darunterliegenden Schicht. Dieser Vorgang wird solange wiederholt, bis das zu druckende Objekt vollständig entstanden ist. Das Objekt wird aus dem Drucker entnommen und das verbleibende Pulver zur Weiterverarbeitung zurückgeführt.
Bei der Binder Jetting Technologie handelt es sich um eine schnelle Fertigungstechnologie, bei der unterschiedliche Materialen eingesetzt werden können. Darunter auch Hilfsstoffe die bereits in der Herstellung pharmazeutischer Darreichungsformen genutzt werden. Vorteilhaft ist zudem, dass durch das Fehlen einer Wärmequelle auch temperaturempfindliche Wirkstoffe verarbeitet werden können. Daher verwundert es nicht, dass das erste 3D gedruckte Arzneimittel (Levetiracetam, Spitram®) durch dieses Verfahren produziert wird. Der Nachteil dieser Technologie besteht darin, dass die gedruckten Objekte nur geringer Belastung standhalten und eine raue Oberfläche aufweisen.
Mit dem Fused Deposition Modeling (FDM)-Verfahren besteht eine weitere Möglichkeit dreidimensionale Objekte zu drucken. Für diese Technologie werden Polymere zu sogenannten Filamenten extrudiert. Diese werden anschließend dem Druckkopf zugeführt und thermisch verflüssigt. Um das gewünschte Objekt zu erhalten, wird die Form schichtweise nach oben aufgebaut, indem entweder der Druckkopf oder der Drucktisch um die gewünschte Schichtdicke vertikal bewegt werden.
Das FDM-Verfahren wird am häufigsten verwendet, da es aktuell kostengünstige 3D-Drucker und Materialien zu beziehen gibt. Die Technologie lässt sich auch für die Herstellung pharmazeutischer Darreichungsformen verwenden. Hierzu wird ein bioabbaubares Polymer wie z.B. Polylactide (PLA) gemeinsam mit dem Wirkstoff zu einem Filament extrudiert, wobei die Auswahl des Polymers und entsprechender Zusatzstoffe die Freisetzungskinetik des Wirkstoffes steuert. Dieser Prozess ist in der pharmazeutischen Industrie seit längerem etabliert.
Für die patientenindividuelle Herstellung oraler Medikamente ist das Fused Deposition Modeling aktuell sicherlich das am meisten geeignete, sinnvollste Verfahren.
FDM bietet wie auch die 2D-Druck-Technologie die Möglichkeit, kosteneffizient, individuelle Chargen mit einer Chargengröße von
n=1 herzustellen. Insbesondere die FDM-Technologie bietet die Chance, mehrere Wirkstoffe mit unterschiedlichen Freisetzungskinetiken in einer gedruckten Tablette herzustellen. Die Entscheidung, welche der beiden Technologien eingesetzt werden kann, hängt maßgeblich von den Spezifikationen der Enddarreichungsform ab. Dazu müssen Parameter wie z.B. Freisetzungskinetiken, Thermostabilität etc. vorab geprüft werden. Die 3D-Druck-Verfahren bieten jedoch den Vorteil einer deutlich höheren Beladung als das 2D-Druck-Verfahren. Ein starker Fokus wird entwicklungstechnisch aktuell darauf gelegt, die Temperaturen im FDM-Druckkopf so gering wie möglich zu halten, um noch mehr Arzneistoffe druckbar zu machen. Sowohl der 2D-Druck wie auch der 3D-Druck sind beim Systemansatz der DiHeSys in einem Druckergehäuse GMP konform umsetzbar (s. Abb. 1).
Aktuelle Beispiele digitaler
Fertigung von Arzneimitteln
Der pharmazeutische 3D-Druck mit seinen oben bereits umrissenen Vorteilen in der Individualmedizin steht seit einigen Jahren im Fokus der Entwicklung und führte im Juli 2015 bereits zur Zulassung des ersten 3D-gedruckten Arzneimittels in den USA. Dabei wird das Arzneimittel „Spritam“ (es enthält das Antiepileptikum Levetiracetam) wie bereits beschrieben in einem Binder Jetting Verfahren hergestellt. Bei „Spitram“ steht die schnelle Freisetzung im Fokus des Interesses, allerdings nicht die Individualisierung.
Die FDM-Technologie ist besonders geeignet für die Individualisierung hochpotenter Wirkstoffe, da der Wirkstoff gebunden im Polymer vorliegt. Aber auch weniger potente Wirkstoffe können mit Hilfe dieser Technologie individualisiert gedruckt werden.
Um auf den Patientennutzen im Kontext der Individualisierung zu fokussieren, schauen wir uns das Beispiel der hochpotenten Tyrosinkinaseinhibitoren an. In dieser Substanzklasse haben viele Wirkstoffe eine geringe therapeutische Breite, müssen also gemäß den klinisch/toxikologischen Entwicklungsdaten sehr genau dosiert werden. Andererseits können Patienten nach dem Stand der Wissenschaft bereits nach ihrem Genotyp bedeutende Unterschiede in der Metabolisierung von Arzneiwirkstoffen aufweisen, hinzu kommen andere Einflussparameter wie z. B. das Geschlecht, das Alter, die Leistungsfähigkeit von Leber und Niere sowie der Allgemeinzustand des Patienten (Fatigue), sodass eine individuelle Dosisreduktion vorteilhaft wäre.
In diversen Fachkliniken, speziell in der Geriatrie und der Pädiatrie, findet die personalisierte Dosierung heute schon verbreitete Anwendung. Insbesondere bei Kindern sind viele Arzneimittel nicht klinisch getestet, weshalb die behandelnden Ärzte zur Vermeidung unerwünschter Arzneimittelwirkungen häufig die Dosis an das Körpergewicht anpassen wollen. Bei Tropfen und Säften ist dies relativ leicht möglich, bei festen Darreichungsformen fehlt bisher die technische Realisierbarkeit. In Kliniken wird hier gerne auf das Verkapseln der Arzneimittel zurückgegriffen, welches in toto nicht genau genug und zudem aufwendig und damit personalintensiv ist. Die digitalen Herstellverfahren bieten hierfür eine mögliche Lösung und werden derzeit getestet.
Ein weiterer wichtiger Vorteil der digitalen Drucktechnologie besteht darin, dass nun auch mehrere Wirkstoffe – auch unabhängig von der jeweiligen Indikation – in patientenindividueller Dosierung in eine Tablette gedruckt werden können (Flexdose Polypill).
Status quo der DiHeSys-Projekte
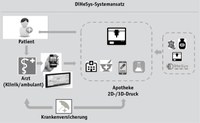
Um die verfahrenstechnologische Machbarkeit, den medizinischen Nutzen und die gesundheitsökonomische Effizienz zu zeigen, werden aktuell in mehreren Gesundheitssystemen (z.B in Deutschland, Österreich, USA) mehrere Pilotprojekte in unterschiedlichen Indikationen und Settings (ambulant und stationär) gestartet, weitere akquiriert. Die aktuellen Projekte umfassen unter anderem die Indikationen Hypertonie, Morbus Parkinson, Prävention des Schlaganfalls und das Glioblastom. Auch werden Dosisfindungsstudien durchgeführt. Die ersten Projekte werden vor allem mit dem 2D-Druckverfahren durchgeführt, da die federführenden Ärzte hier neben der Dosisindividualisierung und des Compoundingansatzes auch die Darreichungsform (ODF, oral dispersibler Film) als Vorteil sehen, da die Einnahme im Gegensatz zu einer Tablette nicht nur bei Patienten mit Dysphagie vorteilhaft erscheint. Weitere Projekte in den Indikationen Immunsuppression, Brustkrebs, Schizophrenie und Depression, Multiple Sklerose, Schmerztherapie und Tumortherapie sind aktuell in der Planung. Auch Kooperationen, die beispielsweise Elemente der künstlichen Intelligenz (z. B. zur optimierten Dosisfindung) mit einbeziehen, oder aber die Korrelation von Talspiegeln, unerwünschten Arzneimittelwirkungen und einer optimierten, weil dosisadaptierten Pharmakotherapie (insbesondere bei Pharmaka mit enger therapeutischer Breite) zum Inhalt haben, werden aktuell diskutiert. Dabei ist relevant, dass die Technologie unabhängig von der Ausgestaltung des jeweiligen Gesundheitssystems eingesetzt werden kann (Abbildung 2). In Systemen, die maßgeblich von gesetzlichen Sozialversicherungssystemen getragen werden, kommen im ambulanten Bereich zunächst selektive Verträge zum Einsatz, aber auch Studien sind geplant. Der Einsatz im stationären Segment umfasst neben der Routine Versorgung ebenfalls den Einsatz im Rahmen von Studien.
Was bringt die Zukunft?
Die neuen digitalen Herstellungsverfahren können zur Individualisierung bzw. zur Personalisierung von Arzneimitteln eingesetzt werden. Damit stehen dem Patienten plötzlich völlig neue Möglichkeiten bei der Individualisierung der Arzneimitteltherapie zur Verfügung, die es vor der Digitalisierungswelle schlichtweg nicht gab. Wie bei innovativen Verfahren üblich, werden vermutlich zukünftig völlig neue Player im Bereich der Medizin und Pharmazie für die Themen Diagnostik, Therapie und Rehabilitation eine Rolle spielen. Die digitalen, innovativen Herstellverfahren, wie der 2D- und 3D-Druck von z.B. Arzneimitteln, Implantaten, Sensoren, Applikationsdevices etc. werden zukünftig leichter verfügbar sein und eine weitaus größere Verbreitung erfahren. Gleichzeitig sehen wir einen Trend zum deutlich mündigeren Patienten, der seine Erkrankung oder sein Wohlbefinden selbstverantwortlicher bestimmen will und als Teil der Gesundheitsindustrie gesehen werden will. Kaum jemand geht heute noch zum Arzt ohne vorher Dr. Google und Co. gefragt zu haben, so kritisch dies im Einzelfall auch sei. Der Patient will mehr Verantwortung übernehmen und mit den neuen Medien und der Digitalisierung ist dies auch leicht möglich.
Der Themenkomplex Arzneimittelsicherheit muss insbesondere bei innovativen Herstellungstechnologien höchste Priorität genießen. Im Dialog mit den Behörden muss die patientenindividuelle Dosierung über den gesamten Therapiebereich erörtert werden.
Im Moment werden gedruckte Tabletten hauptsächlich über Einzelverordnungen rezeptiert und für den einzelnen Patienten personalisiert hergestellt. Letztlich handelt es sich um eine klassische Rezeptur, die de jure unter dem rechtlichen Rahmen der formula magistralis nicht nur innerhalb Europas läuft. Auch Zulassungen von patientenindividuellen Dosierungen sollten bald ermöglicht werden.
Die neue digitale Technologie betrifft uns alle. Der Moment wird kommen, indem die Patienten nach ihren individuell angepassten und somit personalisierten Therapien nachfragen. Diese Nachfrage der Patienten nach bestmöglicher und effizienter Behandlung durch die bestmögliche Therapie mit personalisierten, individualisierten Medikamenten, welche die geringstmöglichen Nebenwirkungen bei schnellstmöglicher Heilung bzw. Linderung verschaffen, wird den Markt bestimmen. Es bleibt zu hoffen, dass alle weiteren Beteiligten der Gesundheitsindustrie wie z.B. Ärzte, Apotheker, Pharmaindustrie, Großhandel, Krankenkasse, Krankenhäuser etc. die Zeichen der Zeit rechtzeitig erkennen. Schließlich sollten zudem bei konsequenter Umsetzung dieser Technologie die Gesamttherapiekosten gesenkt werden. Letztlich sind alle Marktteilnehmer der optimalen Dienstleistung am Patienten verpflichtet und diese Verantwortung wird nur unter Nutzung digitaler und innovativer Technologien wie z.B. dem 2D- und 3D-Druck getragen werden können, um den Patienten human, effizient und optimal behandeln zu können. <<
von:
Prof. Dr. Christian Franken, DiHeSys Digital Health Systems GmbH,
Dr. Markus Dachtler, DiHeSys Digital Health Systems GmbH,
Prof. Dr. Gerald Huber
und Tanja Pries, Gen-Plus
Zitationshinweis:
Franken et al.: „Personalisierte Medikation durch digitalen 2+3D-Druck“, in „Monitor Versorgungsforschung“ (06/20), S. 42-47, doi: 10.24945/MVF.06.20.1866-0533.2262